Topics
2026.03.31 circular No.26
イオン液体の界面を利用した細胞培養物質・材料研究機構 高分子・バイオ材料研究センター
上木 岳士
博士学生の時、芳香族の側鎖をもつ高分子がイオン液体(IL)の中で加熱すると溶けなくなる現象に出会った1。水中では、加熱に伴うタンパク質溶液(例えば卵白)の白濁に見られるように、温度上昇で高分子が溶けなくなる挙動(Lower Critical Solution Temperature: LCST型相転移)はそれほど珍しくない。しかし当時の自分にとって、同じタイプの相転移がILでも起こり得ることは驚きだった。水中でしか起きえないと思っていた現象がイオン液体でも成立する(→後に勘違いだったことを知る2)。ILと生命の繋がりを意識したのは、この頃からだったように思う。
この現象をもう少し勉強すると、加熱すると溶けなくなる高分子水溶液では、高分子のすぐそばで水分子が氷状のクラスター構造を作り、混合のエントロピーを減らしていることを知った3。重要なのは、この構造化によるエントロピー低下が、LCSTを引き起こすための熱力学的な要件になっている、という点である。さらに研究が進むと、博士学生のとき見つけた高分子でも、ILが高分子のすぐそばで構造を作り、同じ役割(エントロピーの低下)を担っていることが見えてきた4, 5。ここで気づかされたのは、水とILのアナロジーである。液体の水は強い水素結合とその幾何構造によって互いに引きつけ合い、単純な分子量で予測されるふるまいから逸脱した物性(沸点、粘度、表面張力等)を示す。ILの特殊な物性の多くも、クーロン相互作用をはじめとする複数の相互作用が重なり合って局所構造をつくることに由来している。そしてこの構造化は、特定の基質導入によって一層、強調される。水では疎水基の導入によって6、ILでは芳香族構造の導入によって7。水とILは同一ではない。ただ、どちらも微視的な構造を内包し、ある種の“異物”と接触することでその構造化が強まる。この点において、水とILはどこか似た雰囲気をもつ。自分はILをそんな風に捉えていた。
IL中で高分子が示すLCSTの実態がつかめてきた頃、自分は物質・材料研究機構(NIMS)のメカノバイオロジーグループに配属された。メカノバイオロジーとは生命現象に及ぼす力学の効果を探求する、比較的新しい学問領域である8-10。この新天地で自分は外部刺激をトリガーとして細胞に力学ストレスを与えるハイドロゲル足場材料に関する研究にアサインされた11-13。研究所では、このようにトップダウンで組織ミッション研究を任されるが、それだけでは埋もれてしまう。プロジェクトに参画しながら、その一方で、遠くから見てもわかるような、自分らしさが見える研究を立ち上げなければならない。NIMSに就職した当時の自分はまったくのバイオの門外漢。頼れる武器は、ILと高分子だけ。折角バイオを学べる環境にきたからには、ILと生命をつなげた独自路線が展開できないかと自らに淡い期待を抱いていた。しかし実際に生命に触れてみると、それまで抱いていた「なんとなく、ILは水と似てるっぽい」という感覚は、とても通用しなかった。とにかく水は、置き換えがきかない。冷静に考えてみると、それはそうだ。水は生命が46億年かけて最適化してきた液体なのだから。Waldenが20世紀の初めに液状のイオン性物質を見つけたといっても、それはたかだが100年前。人類との、いや生命とのつきあいは浅すぎる。水とILのアナロジーから始まった関心は、いつしか水とILの差別化を意識する時期を迎えていた。
IL/バイオ路線では水和ILの研究も成熟しつつある中14、自分は別の切り口で勝負する必要も感じていた。独自路線を模索し、行き着いた先は単純だった。「バイオをやるなら水。でもILも使う。」バイオロジーの土俵で、ILは水に敵わない。だから発想を切り替えよう。水相は水相で、そのままキープ。ILは水の代役ではなく「別のフェーズ」で活かす。ILが得意な領域、つまり構造デザイン性、イオン伝導性、特殊溶解性、に持ち込めば、生命が未経験の化学場/力学場の調整や、その独立制御も見込める。「イオン液体の界面を利用した細胞培養」に関する研究テーマを立ち上げたのは、ちょうど40歳の時だった。
ここではまず、液体界面培養の歴史的背景を説明する。次に“液体”の界面が足場になるとき、細胞が実際に感じているのはなんなのか、ILの化学構造がその環境をどう変え、細胞応答へどう繋がるのかを述べる15。さらに「イオン伝導性のあるIL」、「高分子を溶かせるIL」というILならではの性質を利用した、動的な液体足場のつくり込みを16-18、最後に疎水性ILの細胞毒性に関する機械学習を用いた我々の最近の取り組み19に触れたい。
接着性細胞の培養は、ふつうプラスチックディッシュやガラスのような「固体」界面で行う。細胞は焦点接着(Focal Adhesion: FA)を介して基質に力をかけ、硬さ や張力といった力学情報を読み取りながら、生存、伸展、増殖あるいは分化に関わるシグナルを統合する。ところが近年、疎水性「液体」の界面にも細胞が接着し、その液体界面でヒト幹細胞が選択的に 神経分化したり20、未分化性を維持したりするなど21、興味深い動態が見出されている。応力がミリ秒オーダーで緩和する液体界面で、FA形成を前提とする接着性細胞が生存 を維持できてしまうのだから、とても不思議である。
液体界面における細胞培養の歴史は意外と古い。1964年、Rosenbergはフッ素系液体の界面に細胞が接着、伸展する現象を報告した22。ここで彼が見抜いた本質は「細胞は液体に表面張力をつかって“アメンボのように”張り付いているのではなく、培地(細胞培養に必須なタンパク質が含まれた水溶液、図1(a)上相の赤色液体)から供給されるタンパク質が界面に集積・吸着して、形成する固体薄膜(Protein Nano Layer: PNL)が実体的な足場になっている」という点だった。彼は液体界面培養の核心は実は「液体」ではなく、界面に形成される「薄膜材料」にあることを見抜いていた。事実、1980年代にはKeeseやGiaeverらの体系的な検討によって、PNLが細胞接着を支える実態であることが裏付けられた23-25。彼らは同時にPNLが疎水性液体とタンパク質水溶液の界面張力差を駆動力として“偶発的に”形成される以上、条件によっては力学的に脆弱になり細胞接着を充分に支持できない場合があることも指摘した。これを受け、化学的手段(界面活性剤によって積極的にタンパク変性を誘導する、界面にアンカリングするなど)によってPNLの力学強度を高める方法論がこの時代に複数の研究グループから提案された26-28。こうした戦略はPNLの力学的頑強性を確保するために現在も広く用いられている29-32。しかしその一方、この系譜が示しているのは、液体界面培養の足場が、偶然できあがるPNLに支えられ、その形成と力学が原理的に揺らぎやすいという事実でもある。つまり液体界面培養は重要な学理を獲得しながらも、再現性や操作性の面で実装が難しく、しばらく大きな潮流を生むことはなかった。
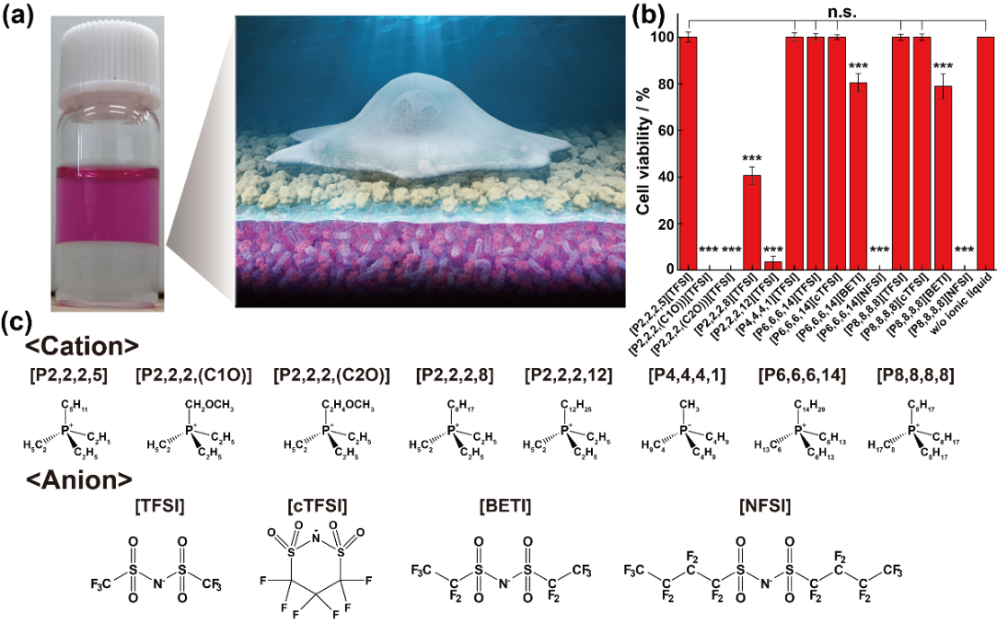
図1 疎水性イオン液体(IL)の細胞毒性評価と化学構造 (a)水相(培地)と疎水性IL相が明確に相分離する界面培養系の概念図(左:二相分離の外観、右:界面に形成される足場環境のイメージ図)。(b) IL飽和培地中で培養した細胞の生存率を指標とした毒性評価の結果。(c) 本研究で評価した疎水性ILの化学構造(カチオン/アニオン)一覧。Wiley社の許可を得て転載。一部改編。
2000年代に入ってから、細胞は周囲の生理化学的要因だけでなく、力学環境を感じ取り、運命を導いていることが徐々に明らかになってきた。メカノバイオロジーの台頭である。細胞は化学的なシグナルだけでなく、硬さ、粘弾性、凹凸、曲率といった構造力学情報を読み取り、形態や遺伝子発現を変える。こうした見方が共有されると、固体足場の「硬さ」を変えるだけで細胞応答が変わるなら、究極に柔らかい液体界面で細胞はどう振る舞うのか、という問いが再び前景化してくる。さらに追い風になったのが、同時期に進んだバイオロジー側の道具立ての発達である。顕微鏡技術の先鋭化は言うまでもなく、超解像、ライブイメージング、ゲノム編集、単一細胞解析など、1980年代には想像しえなかったレベルで細胞の動態が「見え」「測れ」「操作でき」るようになった。こうしてみると液体界面培養は、現象自体は古くから知られていたにもかかわらず、機構に踏み込むための手段が揃わず、どこか“棚上げ”されてきた未完テーマでもあった。いまの状況は、その未完テーマが、ようやく再挑戦に値する題材として再注目され始めた局面かもしれない。(このあたりはWaldenの発見以降のIL研究の歩みにも、どこか似ている。)
以上の流れを受けて近年、液体界面培養に関する研究は、ある種のリバイバルブームが訪れている。しかし現状、我々を除くすべての研究で足場側(サブフェーズ)に用いられているのは、フッ素系液体やシリコーンオイルといった分子性液体である。これら液体は“無毒性で高密度、かつ培地(水溶液)と明確な二相分離界面を形成する”という界面培養に適した性質を持つが、その反面、化学構造は画一的で選択肢の幅は狭い。このためサブフェーズに用いる液体のどのような物性が種々の界面現象、ひいては細胞の動態や運命を決定づけているか不明な点が多かった。「バイオをやるなら水。でもILも使う。」という方針はこの未完点に応えるものである。分子設計自由度の高い疎水性ILは液体足場材料として、原理的に無限の化学構造ライブラリを提供する。高極性でありながら水と相分離し、イオンのみからなる液体の二相分離界面は特殊で、これまで検討されてきた非極性分子性液体とは一線を画したエキゾチックな培養空間を与えることが期待される。さらにILの魅力はイオン伝導性と高分子溶解性を通じて操作可能な足場へ展開できる点にもある。以下ではまず、細胞培養に用いる疎水性ILを選ぶための毒性評価から説明する。
疎水性イオン液体(IL)界面を細胞足場として用いるにあたり、まず越えなければならないのがIL自身の細胞毒性である。疎水性ILは水と相分離するため、水溶性物質のように単純な濃度系列を作って毒性を比較することが難しい(2-6にて後述)。界面培養の実装を考えると、細胞が置かれるのは「疎水性ILが共存する培養環境」であり、培地側はILが溶けうる限り溶け込んだ状態になり得る。そこで我々は、疎水性ILを培地に飽和させた条件で細胞を培養し、その生存率を指標として毒性を評価した。この評価の結果、ホスフォニウム型カチオンを持つ疎水性ILが相対的に高い生存率(低い毒性)を示すという傾向が明確になった(図1(b),(c))。以上を踏まえ、本稿の界面培養パートでは、細胞毒性が低く、界面足場としての検討が可能な代表例として、アルキルホスフォニウム系の[P2,2,2,5][TFSI]、[P4,4,4,1][TFSI]、[P6,6,6,14][TFSI](以下、[P2],[P4],[P6])を選び、界面での細胞接着・伸展挙動へ議論を進める。
2-2. イオン液体界面における細胞の接着、伸展
[P2]、[P4]、[P6]の界面でhMSCs(ヒト間葉系幹細胞)を培養した。図2(a)–(d)に各IL界面およびガラス基板上における細胞の位相差像を示す。結論を先に言えば、IL界面でも細胞は生存し得るだけでなく、伸展する場合としない場合があり、その差がカチオン構造に依存して現れた。位相差像からは、[P4]および[P6]界面では細胞が顕著に広がり、ガラス基板上に近い形態を示す一方、[P2]界面では伸展が抑制され、丸みを帯びた形態が優勢であることが分かる。これらの差は、定量化した細胞面積や伸展度の指標にも反映された(図2(e), (f))。一般に接着性細胞は硬い基質上でより伸展し、柔らかい基質上で丸まりやすい。定性的にhMSCsは[P2]界面を相対的に“柔らかい”足場として感じており、[P4]および[P6]界面を“硬い”足場として感じているように見える。
この解釈を細胞側の指標で確かめるため、FAに集積する代表的タンパク質であるビンキュリンを染色した(図3(a)-(j))。ビンキュリンはインテグリンを介した細胞外マトリックス—アクチン連結部位(図3のF-actin)に集積し、細胞内外のタンパク質同士の結合を強化する「かすがい」のような機能を担うタンパク質である33。[P4]および[P6]では、細胞辺縁部においてアクチン末端にビンキュリンが局在化し、FAが形成されていることが分かる。一方、[P2]ではそのような共局在が明瞭ではない。さらにメカノトランスデューサーであるYAP(細胞が界面を固いと判断すると核内に移行するタンパク質34)の局在を比較すると、[P4]と[P6]では核内移行が見られるのに対し、[P2]では核への局在化は弱い(図3(k)-(o))。以上より、細胞の表現型はサブフェーズに用いるILの種類によって大きく異なることが分かる。すなわちhMSCsは[P2]界面を相対的に柔らかく感じており、[P4]および[P6]界面を硬いと認識しているようである。そこで次に、IL界面に形成されるPNLのキャラクタリゼーションを行った。
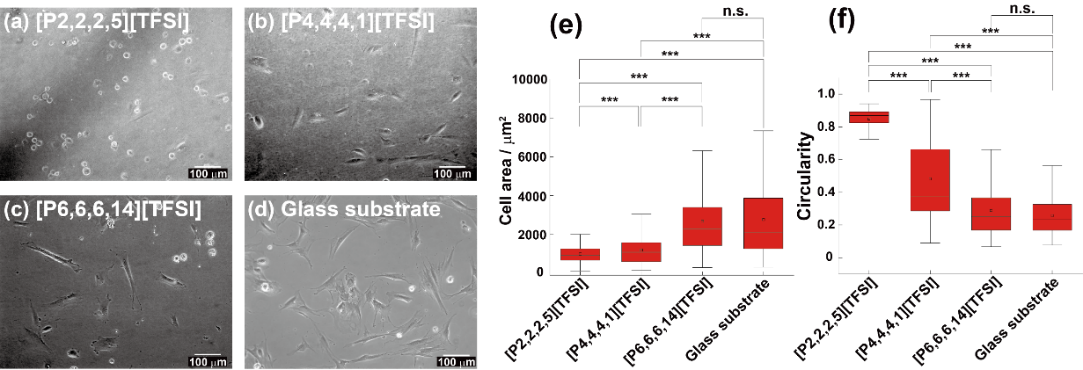
図2 疎水性アルキルホスフォニウム系イオン液体(IL)界面におけるhMSCsの接着・伸展挙動 (a–c) [P2,2,2,5][TFSI]([P2])、[P4,4,4,1][TFSI]([P4])、[P6,6,6,14][TFSI]([P6])界面上で培養したhMSCsの位相差像。(d) 参照としてガラス基板上で培養したhMSCsの位相差像。スケールバーはいずれも100 µm。(e) 各足場上での細胞接着面積の比較。(f) 各足場上での細胞真円度の比較15。Wiley社の許可を得て転載。一部改編。
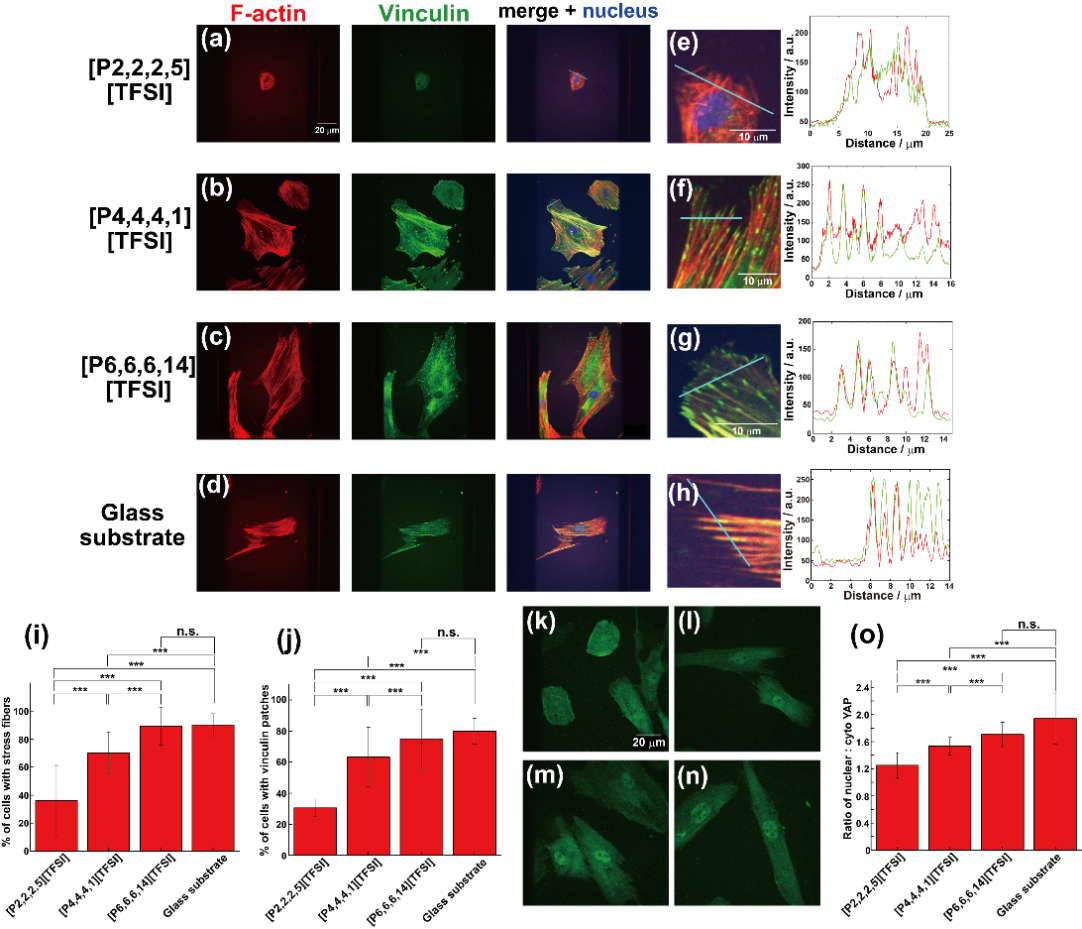
図3 疎水性アルキルホスフォニウム系イオン液体(IL)界面上におけるhMSCsの焦点接着と力学応答の指標 (a–d) [P2]、[P4]、[P6]界面およびガラス基板上で培養したhMSCsの蛍光像(F-actin:赤、ビンキュリン:緑、核:青)。(e–h) 合成像の拡大図と、図中のラインに沿ったF-actin/ビンキュリンの蛍光強度プロファイル。(i, j) ストレスファイバーが形成されている細胞およびビンキュリン集積(パッチ)を示す細胞の割合の定量。(k–n) YAP(Yes-associated protein)染色像([P2]、[P4]、[P6]界面およびガラス基板)。(o) 核内YAP/細胞質YAP比の定量15。Wiley社の許可を得て転載。
2-3. イオン液体界面に形成されるタンパクナノレイヤー
図4(a)、(b)にFITC蛍光色素でラベル化したウシ血清アルブミン(BSA)を接触させた後の[P6]界面の明視野画像と蛍光顕微鏡画像を示す。蛍光顕微鏡像においてのみ液体の界面に明確なクラックがみてとれる。(まるで北極海に浮かぶ氷床のようである。)これは液体界面に固体の薄膜が存在することを示している。PNLの微視的な観察にはAFMを用いた(図4(c)–(k))。同じくBSAを三種類の疎水性ILに接触させてPNLを形成させた。カンチレバーでPNLを矩形に削り取り、露出した平坦な液体界面との段差から厚みを見積もると、PNL厚みは[P2]で約4 nm、[P4]で2.5 nm、[P6]で約1.5 nmと、カチオン構造に従って薄くなる傾向を示した(図4(e),(h),(k))。BSA短軸長(~3 nm)を踏まえると、少なくとも界面では単分子層程度の吸着が示唆される。一方、AFMナノインデンテーションにより見かけのヤング率を評価すると、力学特性は大きく変化した。見かけのヤング率は15.0 kPa([P2])、30.6 kPa([P4])、45.9 kPa([P6])となり、IL構造に従って2〜3倍変化した(図4(l))。この序列は2-2で見たhMSCsの伸展度の序列と整合しており、細胞表現型がPNL力学を介して変わっているという見立てを支持する。
分子性液体界面では、PNLの厚み・力学はバルク極性に依存し、低極性界面ほど吸着変性が強く薄く硬いPNLになりやすいという描像が知られている35-37。今回のIL系でも、[P2]→[P4]→[P6]でPNLは薄く硬くなり、より強い吸着変性が示唆された。実際、FT-IR(ATR)でアミドI/II強度比を指標として扱うと、比は[P6] < [P4] < [P2]となり、[P6]では吸着変性が強く進行すると解釈できる(図4(m))。しかし極性指標ET(30)は47.4([P2])~46.6([P4])~45.5([P6]) kcal mol⁻¹と差が小さく、これだけでヤング率の2〜3倍変化を説明するのは難しい。したがってIL界面では、バルク極性以外の因子がPNL形成を後押ししている可能性が高いと考えられた。そこで次にPNL形成プロセスそのものを高速AFMで可視化した。
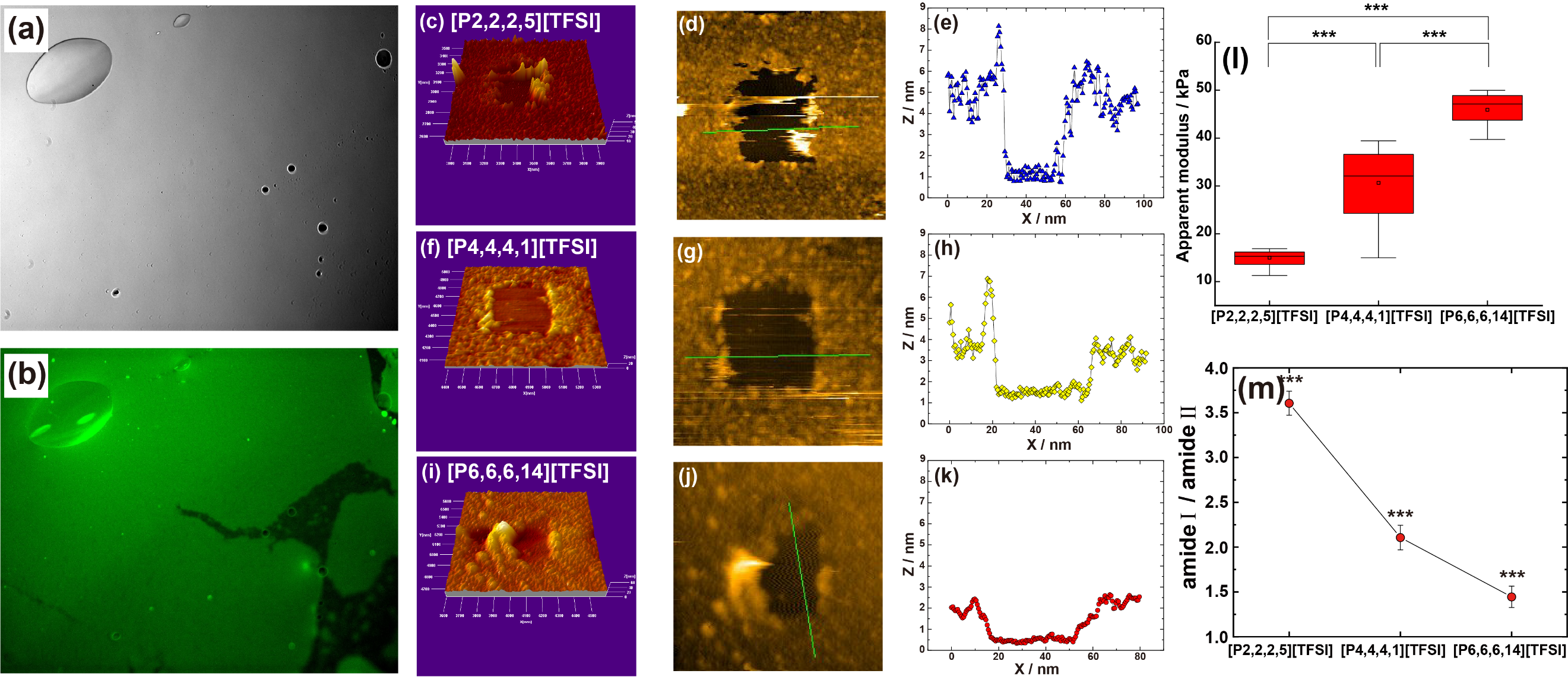
図4 疎水性IL界面に形成されるプロテインナノレイヤー(PNL)のキャラクタリゼーション FITC蛍光色素でラベル化したBSAを接触させた後の[P6]界面における(a)明視野画像と(b)蛍光画像。 (c–e) [P2]界面に形成したPNLのAFM像(3D表示)、カンチレバーによるスクラッチ後の観察像、およびラインプロファイル(高さプロファイル)。(f–h) [P4]界面で形成したPNLのAFM像(3D表示)、スクラッチ後の観察像、および高さプロファイル。(i–k) [P6]界面で形成したPNLのAFM像(3D表示)、スクラッチ後の観察像、および高さプロファイル。(l) AFMナノインデンテーションにより評価したPNLの見かけの弾性率(ヤング率)の比較。(m) ATR-IRにより評価したBSA由来アミドI/アミドII強度比(I/II)の比較(吸着変性の指標)15。Wiley社の許可を得て転載。
2-4. 高速AFMによるPNL形成プロセス図5(a)–(l)に、PNLが形成していく様子を各IL界面・各時間のスナップショットとして示す。白い点状に見えるのがBSA粒子である。いずれの界面でも、時間経過とともに界面が徐々にBSAで覆われていく様子が確認できる。ここで興味深いのは、溶液バルクから拡散してきたBSA粒子がIL界面に接触した瞬間、吸着と同時に、その場で固定されるのではなく、界面上でブラウン運動(2次元拡散)した後に動きを止める点である。しかもそのダイナミックスはILの種類に依存して変化する(静止画ではわかりにくいが、原著15からアクセスできる動画を参照して頂きたい)。この点を定量化するため、高速AFMの画像解析からBSAの重心位置を追跡し、軌跡をトレースした(図5(m)–(o))。BSAの二次元拡散はIL構造に応じて明確に変化する。そこで平均二乗変位と時間の関係から、界面におけるBSAの二次元拡散係数Dを算出した(図5(p))。結論としてDはIL構造に従って1〜2桁の広い範囲で変化した(D = 1.71 × 10⁻¹⁰ cm² s⁻¹([P2])、6.18 × 10⁻¹¹ cm² s⁻¹([P4])、3.73 × 10⁻¹² cm² s⁻¹([P6]))。さらに重要なのは、この拡散係数の序列がPNLの見かけのヤング率の序列と逆相関にあった点である。すなわち、吸着初期におけるダイナミックスの違いこそが、PNLの見かけのヤング率にして2〜3倍にも及ぶ力学強度差を生んでいる可能性が高いと考えられた。この結果から我々は、[P6]界面ではBSAが界面に接触した直後から吸着変性が進み、内部の疎水性アミノ酸が露出し、界面との引力的相互作用(疎水性相互作用)が強く働いていると考えた。タンパク質内部の疎水性領域と界面との相互作用は、界面上での2次元拡散に対する抵抗成分として働き、ブラウン運動を強く抑制する。その結果として拡散係数が低下し、強い変性が起きるためにより硬いPNLが形成される。対照的に、[P2]界面では界面変性の程度が相対的に小さく、BSAはより自由に拡散できるため高い拡散係数を与える。言い換えると、IL界面におけるPNLの力学特性は、バルク極性のような単純な指標だけで決まるのではなく、ILの配向を反映した界面に構造化した局所環境が強く効いているということである15。この界面局所における構造化は最近のNishiらの研究結果によっても支持される38。トリオクチルメチルアンモニウム ノナフルオロブタンスルフォンイミド([N8,8,8,1][NFSI])と水が形成する界面において、[N8,8,8,1]カチオンがオクチル基よりも極性の高いメチル基を界面に向ける傾向を示し、結果として界面がメチル基リッチになることを明らかにした。これを本系に当てはめると、[P6]ではカチオン構造中のアルキル鎖がいずれも長く、界面はより長鎖アルキルリッチになりやすいと想像できる。逆に[P2]や[P4]ではカチオン中にエチル基やメチル基を含むため、水との接触界面では、その界面エネルギーを下げるべく短鎖アルキルのリッチな界面が露出し、タンパク質がよりソフトに吸着する環境が現れていると考えられた。

図5 高速AFMによるBSA吸着過程の可視化と界面二次元拡散ダイナミクスの定量
(a–d) [P2]界面におけるBSA吸着過程の高速AFMスナップショット(0、100、200、300 s)。(e–h) [P4]界面におけるBSA吸着過程の高速AFMスナップショット(0、100、200、400 s)。(i–l) [P6]界面におけるBSA吸着過程の高速AFMスナップショット(0、100、200、400 s)。(m–o) 各IL界面における高速AFM像の粒子追跡解析により得られたBSA粒子の界面上ブラウン運動。(p) 平均二乗変位と時間の関係から算出したBSA粒子の界面二次元拡散係数Dの比較15。Wiley社の許可を得て転載。
これまでにIL界面におけるPNL形成が、吸着初期のタンパク質ダイナミックスと界面局所環境に強く支配されることを示した。しかし、PNLが界面に立ち上がる薄膜材料である以上、その力学特性を狙って強化し、必要に応じてスイッチングできるかどうかが、液体界面培養を単純な現象から操作可能な足場プラットフォームへ引き上げる鍵になる。1-2で述べたように、従来、界面活性剤や反応性試薬などの化学添加によってPNLを補強する手法が主流であったが、細胞を扱う実験系としてはわずかな残留成分の毒性や、反応の非選択性、不可逆性が問題になる。この点で、ILが本質的に持つイオン伝導性は強力な武器になる。液|液界面に電位を印加すれば、界面近傍のイオン組成・配向をその場で変え、PNLの構造と粘弾性を界面スペシフィックに操作できる。実際、PNL形成後に電位を切り替えても吸着量の変化は小さい一方、界面レオロジーで観測される力学応答は大きく変化し、しかも可逆にスイッチングできることが確認された(図6)。これは、電位印加によって界面に集積するイオンとタンパク質(負に帯電したBSA)との相互作用が吸着変性と分子間相互作用を促進し、PNL内部の擬二次元のネットワークを強めるためと解釈できる。電気化学刺激が細胞培養系にとって魅力的なのは、その生理的親和性と観察手法との直交性にある。光刺激は蛍光プローブや観察波長とバッティングしうるが、電気刺激は光による細胞観察との直交性(光プローブとの競合回避)に優れる。本系を活用することで、界面力学をスイッチしながら、細胞形態、FA関連タンパク質の挙動、YAP核移行などをリアルタイムで追跡する、動的メカノバイオロジーのためのプラットフォームとしても展開可能と考え、現在も検討を続けている16。

図6 電気化学的刺激によるPNL力学の可逆制御(概念図と界面レオロジー) (a)疎水性IL−水界面に形成されたPNLに対し、界面電位差を印加して界面近傍のイオン環境(配向・集積)を変調し、PNLの二次元粘弾性を制御する概念図。(b)界面レオロジーにより測定したPNLの貯蔵弾性率G′と損失弾性率G′′の電位応答。青色領域は-0.6V、赤色領域は+0.3V印加時を示し、電位切り替えに伴って界面粘弾性が可逆的にスイッチングすることを示す16。
2-6. イオンゲルの利用
さて本節では、界面修飾とは異なるアプローチで、細胞伸展の安定化、ひいては表現型の制御に成功した結果を示す。キーポイントになったのは、ILが高分子(ゲル)に対して示す高い溶解(膨潤)性である。細胞培養でよく用いられるパーフルオロオクタン(PFO)やパーフルオロデカリン(PFD)のような液体は決して高分子を溶解しないが、ここで用いたアルキルホスフォニウム系の細胞無毒性ILはポリメタ(ア)クリル酸類や一部のポリアクリルアミド類など、広範な汎用高分子構造に対して優れた溶解性を示した。我々はその中でも、ポリ(メタクリル酸n-ブチル)(PnBuMA)を選択し、これを用いたラジカル重合により、化学架橋イオンゲルを合成した(図7(a))。本イオンゲルを足場としてhMSCsを培養した結果を図7(b)に示す。[P2]の液体そのもので培養した場合とは状況が大きく異なり、ILをゲル化することで細胞がよく伸展するようになることが分かる。液体界面とゲル界面で培養したときの細胞伸展面積および真円度を比較すると、伸展度は明らかに増大した(図7(c), (d))。もちろん、ILで膨潤したイオンゲルと、ILそのもので界面の状態が厳密に同一かどうかは議論の余地がある。それでも本結果は、界面(すなわちPNL)そのものに直接手を加えることなく、疎水性の液体を高分子網目と複合化し、バルク側の力学特性をチューニングすることで細胞表現型を変調し得ることを示す。今回は詳述しないが、溶解させる高分子自体に刺激応答性を組み込み、光刺激によって足場そのものの粘弾性を可逆変化できる動的足場材料の展開も進めている(図8)17, 18。
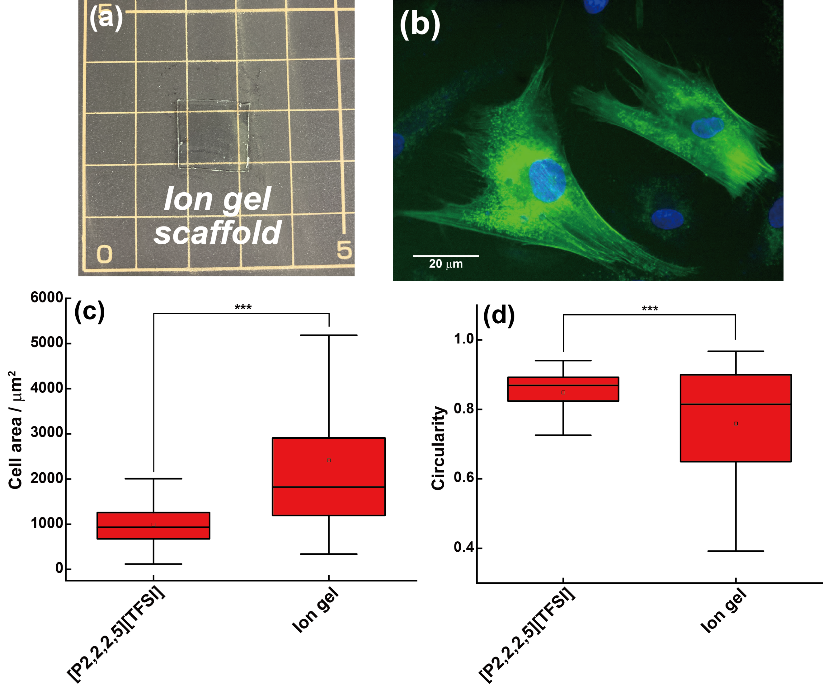
図7 イオンゲル化による足場バルク力学の導入とhMSCs伸展の安定化 (a) [P2] 中で、n-ブチルメタクリレート(nBuMA)をその場ラジカル重合して得た化学架橋イオンゲルの外観写真。(b) [P2]–PnBuMA イオンゲル界面上に接着・伸展したhMSCs(LifeAct-GFP;核は青)の蛍光像(スケールバー:20 µm)。(c, d) [P2] 液体界面と [P2]–PnBuMA イオンゲル界面で培養したhMSCsの細胞面積および真円度の比較15。Wiley社の許可を得て転載。

図8 光刺激によるイオン液体足場のバルク粘弾性スイッチングと細胞応答 (a) アゾベンゼン含有高分子を用いた光誘起ゾル–ゲル可逆スイッチング 18。 (b) 細胞無毒性イオン液体中で形成したアゾベンゼン含有イオンゲルの外観および(c)その界面で伸展した細胞像(赤:F-actin、青:核; スケールバー:100 µm) 18。(d) 可視光(青/緑)照射により液体足場(高分子/IL系)の粘度(粘弾性)を可逆にスイッチングできることを示すイメージ図17。Wiley社およびRSCの許可を得て転載。
2-7. 細胞毒性と機械学習
さて、2-1で述べたように細胞培養系にILを共存させようとしたとき、まず超えるべきはその細胞毒性である。カチオンとアニオンを独立設計できるILは候補数が膨大であり、勘と試行錯誤だけで「使える系」に辿り着くのは現実的ではない。そこで我々は、データ駆動(機械学習による回帰)と最小限の実験を往復させる形で、界面細胞培養に使える細胞無毒性ILの探索と分子論の抽出を試みた(図9(a),(b))。ここで重要なのは、界面培養で問題になる毒性の見え方が、一般的なEC50/IC50の議論とは少し異なる点である。本培養系において細胞は疎水性相と連続的に接し、培地側はその液体が溶けうる限り溶け込むため、議論すべきは希薄溶液でのpotency(力価, 図9(c))というより、実使用条件に近い濃度域で生存できるかというefficacy(有効性, 図9(d))寄りの尺度になる。この前提に立つと、従来よく言われる「カチオンのアルキル鎖が長いほど毒性が上がる」という単純な相関だけでは整理できず、「疎水性=単純な長鎖化」ではなく「疎水性の作り方(分岐のさせ方)」が効くことが見えてきた。一本鎖の長鎖化は生存率を下げやすい一方、多分岐(複数の長鎖アルキルカチオン)構造は同程度の疎水性を保ちながら相対的に毒性が低くなる傾向を示し得る。ホスフォニウムでもアンモニウムでも、この考えは成り立つ。一例として、[N6,6,6,2][TFSI]のような多分岐アンモニウム構造が、界面培養条件下で生存率を確保しやすい候補として機械学習による検討から見出された19。
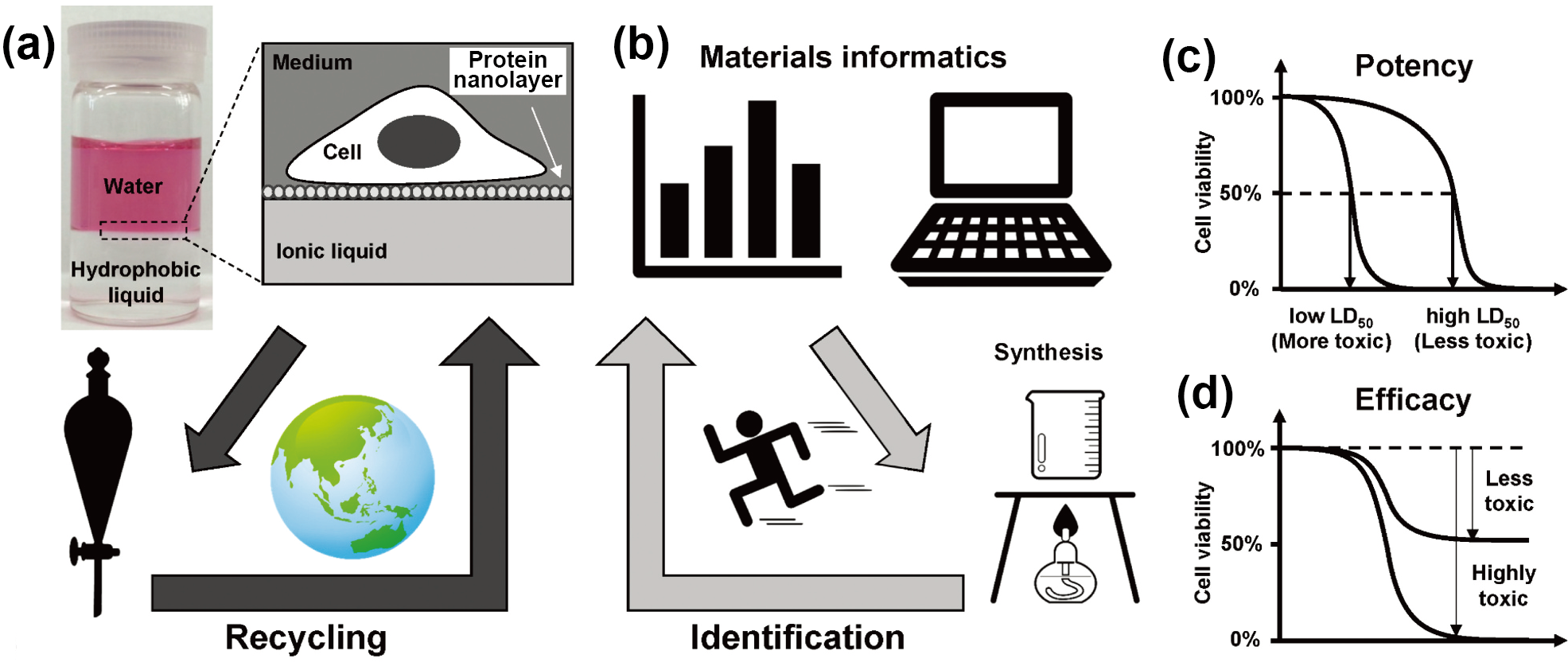
図9 材料インフォマティクス(MI)を用いた疎水性イオン液体の細胞適合設計の概念図 (a) 水相/リサイクル可能なIL相が形成する二相界面における細胞培養の模式図。(b) MI(データ解析・予測)と合成・評価実験を往復させることで、低毒性IL候補を効率よく同定する研究フロー(探索→同定→リサイクルの循環を含む)。(c) 従来の毒性評価指標であるpotency(LD50)の概念図。(d) 界面培養条件に即したefficacy(飽和溶解条件下での生存率)による評価概念図(同じLD50でも実使用条件での毒性が異なり得ることを示す) 19。Taylor & Francis社の許可を得て転載。
ここで強調したいのは、設計指針そのものに加えて、探索の帰結が実装面の可能性を大きく広げた点である。界面培養の初期段階では、細胞無毒性を満たす疎水性ILは[P2]、[P4]、[P6]などのアルキルホスフォニウム系に限られると、我々自身が半ば「思い込んで」いた。ところが機械学習と実験の往復を進めると、同様に“多分岐・長鎖”の設計思想を持つアルキルアンモニウム系(例:[N6,6,6,2][TFSI])でも、細胞毒性が低く液体足場として適用可能な候補が現実に見出された。これは候補が増えただけでなく、前駆体の扱いという観点から構造アクセス性を格段に広げる。毒性があり高酸化(場合によっては発火)リスクを伴う、扱いづらさがあるアルキルホスフィンを要するホスフォニウム系に対し、アルキルアミンを前駆体にできるアンモニウム系は合成・安全・供給の面で有利である。すなわち、毒性を満たす疎水性ILの設計空間がホスフォニウム中心からアンモニウムへも拡張されたことは、液体足場材料としての現実的な展開可能性を一段押し広げた。
本稿では、疎水性イオン液体(IL)−水界面を細胞足場として利用する試みを、界面現象から材料設計まで一気通貫で述べた。接着性細胞が液体界面に接着できてしまうという一見、直感に反する現象は、PNLという薄膜材料の存在によって理解される。一方でPNLは界面で自発的に形成されるがゆえに条件依存性と揺らぎを抱え、細胞足場として使いこなすには形成と力学を材料として昇華させる必要が残されていた。ILは水と相分離しながら高極性で、しかも二成分(カチオンとアニオン)の独立した要素からなる液体であり、PNLの形成プロセスと材料特性を足場側から作り分ける設計空間を与える。実際にアルキルホスフォニウム系IL界面では、細胞が伸展する場合としない場合が現れ、その差はカチオン構造に依存して変化した。PNLの見かけのヤング率は2〜3倍変化し、その序列は細胞伸展と整合した。さらに高速AFMにより、吸着初期におけるタンパク質の二次元拡散ダイナミックスがIL構造で1〜2桁変化することを直接可視化し、その速度論が最終的なPNLの力学と強く結びつくことを示した。
さらに本稿ではILを「設計できる足場」に留めず「操作できる足場」へ押し広げる二つの軸を示した。ILのイオン伝導性は界面(PNL)を電気化学的にクリーンかつ可逆に補強・スイッチングする軸を与え16、ILの高分子溶解性はイオンゲル化や光応答性高分子17・ブロック共重合体の導入18によってバルク粘弾性を設計・スイッチングする軸を与える。これらは、従来のフッ素系液体やシリコーンオイルのような非イオン伝導性、低(無)極性の分子性液体足場では原理的に持ち得ない操作自由度である。一方、実装に向けた最初の関門は細胞毒性であり、設計空間の広いILでは経験則だけで探索するのは現実的ではない。そこで我々は、界面培養という使用状況に即した毒性評価とデータ駆動(機械学習)を往復させ、低毒性ILの探索と分子論の抽出を試みた。その結果、従来のアルキルホスフォニウム系に加え、複数の長鎖アルキルアンモニウム系ILも界面足場材料に適用可能であることが見えてきた。液体界面培養は、幹細胞培養の効率化や操作性の観点からエマルジョン分散培養19, 30, 39やフロー培養系へ展開し得る。PFAS問題でフッ素系液体の環境残留性が懸念されるなか、蒸気圧が極めて低く、回収・洗浄・乾熱滅菌を含むリユースが可能なIL足場は環境適合性の面でも合目的である。
博士学生の時、頭の片隅に残ったのは「ILは(高)分子を“構造化”させうる場だ」という感覚だった。溶媒和の組み替えが高分子の状態を切り替えるなら、界面という究極の不均一場では、その構造化はもっと露骨になる。水との差別化を考え抜いた結果、恐る恐る手を出したイオン液体の界面を利用した細胞培養は、今なお自分の中では学生時代の感覚の延長線上にある。学生時代に見ていたのは、高分子の周りでILが構造化し、混合のエントロピーを押し下げて相転移を駆動する、というバルクの熱力学だった。いま見ているのは、その構造化が界面で顕在化し、細胞表現型に届くという、やはり局所構造が駆動する階層的な現象の連鎖である。ILの化学構造が決まると、界面でのイオン配向が決まり、局所環境が決まる。すると、タンパク質の二次元拡散や吸着変性といったダイナミクスが変わり、平衡状態としてのPNLの力学(粘弾性・見かけのヤング率)につながる。そして最終的にできてくるPNLの性質によって細胞が感じ取る“足場”の性格が変わる。少し乱暴な言い方をすればILの構造選択性が生命のあり方を支配している。「風が吹けば桶屋が儲かる」的な因果連鎖が、ILの界面で確かに起きている。だからこそ、界面を偶然に任せず、設計し、さらに操作するという発想が、これから意味を持つのだと思う。界面は電気化学、バルクは高分子設計、毒性はデータ駆動で。IL界面は、学理と方法論が同時に育つ「足場」だと感じている。
本稿で紹介した研究は、多くの共同研究者・研究室メンバーの支えによって進めてきました。液体界面培養に関して中西淳グループリーダー、宇都甲一郎主幹研究員、山本翔太研究員(NIMS)に感謝します。電気化学的界面制御に関して西直哉准教授、石井浩介博士(現所属・KEK)(京都大学)に感謝します。イオンゲルの光スイッチングは、猿渡彩博士(現所属・東京大学)(北海道大学)の研究成果です。機械学習によるILの毒性評価に関して袖山慶太郎グループリーダー、Dieb Sae主任研究員、野口秀典主席研究員(NIMS)に感謝します。なお本研究は、科研費 基盤B(20H02804、23H02030、23K26726)および挑戦的研究(萌芽)(20K21229)の支援を受けて実施しました。
参考文献
- Ueki, T.; Watanabe, M. Lower critical solution temperature behavior of linear polymers in ionic liquids and the corresponding volume phase transition of polymer gels. Langmuir 2007, 23 , 988-990. DOI: 10.1021/la062986h.
- Somcynsky, T. The Lower Critical Solution Temperature (LCST) of Non-Polar Polymer Solutions: An Introduction. Polym. Eng. and Sci. 1982, 22, 58-63.
- Schild, H. Poly (N-isopropylacrylamide): experiment, theory and application. Prog. Polym. Sci. 1992, 17 , 163-249.
- Matsugami, M.; Fujii, K.; Ueki, T.; Kitazawa, Y.; Umebayashi, Y.; Watanabe, M.; Shibayama, M. Specific solvation of benzyl methacrylate in 1-ethyl-3-methylimidazolium bis(trifluoromethane sulfonyl)amide ionic liquid. Anal. Sci. 2013, 29, 311-314.
- Fujii, K.; Ueki, T.; Hashimoto, K.; Kobayashi, Y.; Kitazawa, Y.; Hirosawa, K.; Matsugami, M.; Ohara, K.; Watanabe, M.; Shibayama, M. Microscopic Structure of Solvated Poly(benzyl methacrylate) in an Imidazolium-Based Ionic Liquid: High-Energy X-ray Total Scattering and All-Atom MD Simulation Study. Macromolecules 2017, 50, 4780-4786. DOI: 10.1021/acs.macromol.7b00840.
- Widom, B.; Bhimalapuram, P.; Koga, K. The hydrophobic effect. Physical Chemistry Chemical Physics 2003, 5 . DOI: 10.1039/b304038k.
- Deetlefs, M.; Hardacre, C.; Nieuwenhuyzen, M.; Sheppard, O.; Soper, A. K. Structure of ionic liquid-benzene mixtures. J. Phys. Chem. B 2005, 109 , 1593-1598. DOI: 10.1021/jp047742p.
- Ingber, D. E. Mechanobiology and diseases of mechanotransduction. Ann Med 2003, 35, 564-577. DOI: 10.1080/07853890310016333.
- Chaudhuri, O.; Cooper-White, J.; Janmey, P. A.; Mooney, D. J.; Shenoy, V. B. Effects of extracellular matrix viscoelasticity on cellular behaviour. Nature 2020, 584, 535-546. DOI: 10.1038/s41586-020-2612-2.
- Engler, A. J.; Sen, S.; Sweeney, H. L.; Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell 2006, 126, 677-689. DOI: 10.1016/j.cell.2006.06.044.
- Homma, K.; Chang, A. C.; Yamamoto, S.; Tamate, R.; Ueki, T.; Nakanishi, J. Design of azobenzene-bearing hydrogel with photoswitchable mechanics driven by photo-induced phase transition for in vitro disease modeling. Acta Biomater 2021,132,103-113. DOI: 10.1016/j.actbio.2021.03.028.
- Homma, K.; Chang, A. C.; Yamamoto, S.; Ueki, T.; Nakanishi, J. Polarity does not matter: Molecular weight reverses the photoisomerization-induced phase separation of an azobenzene-bearing polymer. Macromol. Rapid Commun. 2023, 44, 2300118. DOI: 10.1002/marc.202300118.
- Ueki, T.; Osaka, Y.; Homma, K.; Yamamoto, S.; Saruwatari, A.; Wang, H.; Kamimura, M.; Nakanishi, J. Reversible Solubility Switching of a Polymer Triggered by Visible-Light Responsive Azobenzene Photochromism with Negligible Thermal Relaxation. Macromol Rapid Commun 2024, 45, e2400419. DOI: 10.1002/marc.202400419.
- Fujita, K.; Ohno, H. Hydrated Ionic Liquids: Perspective for Bioscience. Chem Rec 2023, 23, e202200282. DOI: 10.1002/tcr.202200282.
- Ueki, T.; Uto, K.; Yamamoto, S.; Tamate, R.; Kamiyama, Y.; Jia, X.; Noguchi, H.; Minami, K.; Ariga, K.; Wang, H.; et al. Ionic Liquid Interface as a Cell Scaffold. Adv Mater 2024, 36, 2310105. DOI: 10.1002/adma.202310105.
- Ishii, K.; Ueki, T.; Nakanishi, J.; Akutsu-Suyama, K.; Yamada, N. L.; Yokoyama, Y.; Sakka, T.; Nishi, N. Potential-Switchable Viscoelasticity of Protein Nanolayers at a Liquid/Liquid Interface. Langmuir 2025, 41 , 17973-17981. DOI: 10.1021/acs.langmuir.5c01819.
- Saruwatari, A.; Kamiyama, Y.; Nakanishi, J.; Tamate, R.; Ueki, T. Stimuli-responsive liquid cell scaffold: reversible viscoelasticity switching of a polymer in an ionic liquid by visible-light. Polymer Chemistry 2026, 17 , 310-324. DOI: 10.1039/d5py00876j.
- Saruwatari, A.; Kamiyama, Y.; Tamate, R.; Nakanishi, J.; Ueki, T. Toward Dynamic Liquid Cell Scaffold: Photoreversible Ion Gels Exhibiting Light-Induced Sol-Gel Transitions. Macromol Rapid Commun 2026, e00909. DOI: 10.1002/marc.202500909.
- Nakanishi, J.; Ueki, T.; Dieb, S.; Noguchi, H.; Yamamoto, S.; Sodeyama, K. Data-driven optimization of the in silico design of ionic liquids as interfacial cell culture fluids. Sci Technol Adv Mater 2024, 25, 2418287. DOI: 10.1080/14686996.2024.2418287.
- Jia, X.; Minami, K.; Uto, K.; Chang, A. C.; Hill, J. P.; Nakanishi, J.; Ariga, K. Adaptive Liquid Interfacially Assembled Protein Nanosheets for Guiding Mesenchymal Stem Cell Fate. Adv Mater 2020, 32 , e1905942. DOI: 10.1002/adma.201905942.
- Jia, X.; Song, J.; Lv, W.; Hill, J. P.; Nakanishi, J.; Ariga, K. Adaptive liquid interfaces induce neuronal differentiation of mesenchymal stem cells through lipid raft assembly. Nature Communications 2022, 13 , 3110. DOI: 10.1038/s41467-022-30622-y.
- Rosenberg, M. D. Cell surface interactions and interfacial dynamics; Elsevier, 1964.
- Giaever, I.; Keese, C. R. Behavior of cells at fluid interfaces. Proceedings of the National Academy of Sciences of the United States of America 1983, 80, 219-222.
- Keese, C. R.; Giaever, I. Cell growth on liquid interfaces: Role of surface active compounds. Proceedings of the National Academy of Sciences of the United States of America 1983, 80, 5622-5626.
- Keese, C. R.; Giaever, I. Cell growth on liquid microcarriers. Science 1983, 219, 1448-1449.
- Keese, C. R.; Giaever, I. Substrate mechanics and cell spreading. Experimental Cell Research 1991, 195, 528-532.
- Shiba, Y.; Ohshima, T.; Sato, M. Growth and morphology of anchorage-dependent animal cells in a liquid/liquid interface system. Biotechnology and Bioengineering 1998, 57, 583-589.
- Shiba, Y.; Ohshima, T.; Sato, M. Effect of surface active compounds on growth and adhesion of anchorage-dependent animal cells at liquid/liquid interface. Kagaku Kogaku Ronbunshu 1998, 24, 343-345.
- Kong, D.; Nguyen, K. D. Q.; Megone, W.; Peng, L.; Gautrot, J. E. The culture of HaCaT cells on liquid substrates is mediated by a mechanically strong liquid-liquid interface. Faraday Discuss 2017, 204, 367-381. DOI: 10.1039/c7fd00091j.
- Kong, D.; Peng, L.; Di Cio, S.; Novak, P.; Gautrot, J. E. Stem Cell Expansion and Fate Decision on Liquid Substrates Are Regulated by Self-Assembled Nanosheets. ACS Nano 2018, 12 (9), 9206-9213. DOI: 10.1021/acsnano.8b03865.
- Kong, D.; Megone, W.; Nguyen, K. D. Q.; Di Cio, S.; Ramstedt, M.; Gautrot, J. E. Protein Nanosheet Mechanics Controls Cell Adhesion and Expansion on Low-Viscosity Liquids. Nano Lett. 2018, 18, 1946-1951. DOI: 10.1021/acs.nanolett.7b05339.
- Kong, D.; Peng, L.; Bosch-Fortea, M.; Chrysanthou, A.; Alexis, C. V. J.; Matellan, C.; Zarbakhsh, A.; Mastroianni, G.; Del Rio Hernandez, A.; Gautrot, J. E. Impact of the multiscale viscoelasticity of quasi-2D self-assembled protein networks on stem cell expansion at liquid interfaces. Biomaterials 2022, 284, 121494. DOI: 10.1016/j.biomaterials.2022.121494.
- Balaban, N. Q.; Schwarz, U. S.; Riveline, D.; Goichberg, P.; Tzur, G.; Sabanay, I.; Mahalu, D.; Safran, S.; Bershadsky, A.; Addadi, L.; et al. Force and focal adhesion assembly: A close relationship studied using elastic micropatterned substrates. Nat. Cell Biology 2001, 3, 466-472.
- Dupont, S.; Morsut, L.; Aragona, M.; Enzo, E.; Giulitti, S.; Cordenonsi, M.; Zanconato, F.; Le Digabel, J.; Forcato, M.; Bicciato, S.; et al. Role of YAP/TAZ in mechanotransduction. Nature 2011, 474, 179-183. DOI: 10.1038/nature10137.
- Bergfreund, J.; Bertsch, P.; Fischer, P. Adsorption of proteins to fluid interfaces: Role of the hydrophobic subphase. Journal of Colloid and Interface Science 2021, 584, 411-417. DOI: 10.1016/j.jcis.2020.09.118.
- Bergfreund, J.; Diener, M.; Geue, T.; Nussbaum, N.; Kummer, N.; Bertsch, P.; Nystrom, G.; Fischer, P. Globular protein assembly and network formation at fluid interfaces: effect of oil. Soft Matter 2021, 17 , 1692-1700. DOI: 10.1039/d0sm01870h.
- Bergfreund, J.; Bertsch, P.; Fischer, P. Effect of the hydrophobic phase on interfacial phenomena of surfactants, proteins, and particles at fluid interfaces. Current Opinion in Colloid & Interface Science 2021, 56. DOI: 10.1016/j.cocis.2021.101509.
- Ishii, K.; Sakka, T.; Nishi, N. Potential dependence of the ionic structure at the ionic liquid/water interface studied using MD simulation. Physical Chemistry Chemical Physics 2021, 23, 22367-22374. DOI: 10.1039/d1cp02484a.
- Peng, L.; Gautrot, J. E. Long term expansion profile of mesenchymal stromal cells at protein nanosheet-stabilised bioemulsions for next generation cell culture microcarriers. Mater Today Bio 2021, 12, 100159. DOI: 10.1016/j.mtbio.2021.100159.
